Как обозначается постоянная больцмана. Людвиг Больцман: Именные достижения
Среди фундаментальных постоянных постоянная Больцмана k занимает особое место. Ещё в 1899 г. М. Планк предлагал следующие четыре числовых константы в качестве фундаментальных для построения единой физики: скорость света c , квант действия h , гравитационную постоянную G и постоянную Больцмана k . Среди этих констант k занимает особое место. Она не определяет элементарных физических процессов и не входит в основные принципы динамики, но устанавливает связь между микроскопическими динамическими явлениями и макроскопическими характеристиками состояния частиц. Она же входит в фундаментальный закон природы, связывающий энтропию системы S с термодинамической вероятностью её состояния W :
S=klnW (формула Больцмана)
и определяющий направленность физических процессов в природе. Особое внимание следует обратить на то, что появление постоянной Больцмана в той или иной формуле классической физики всякий раз совершенно отчётливо указывает на статистический характер описываемого ею явления. Понимание физической сущности постоянной Больцмана требует вскрытия громадных пластов физики - статистики и термодинамики, теории эволюции и космогонии.
Исследования Л. Больцмана
Начиная с 1866 г. Одна за другой выходят в свет работы австрийского теоретика Л. Больцмана. В них статистическая теория получает столь солидное обоснование, что превращается в подлинную науку о физических свойствах коллективов частиц.
Распределение было получено Максвеллом для простейшего случая одноатомного идеального газа. В 1868 г. Больцман показывает, что и многоатомные газы в состоянии равновесия будут также описываться распределением Максвелла.
Больцман развивает в трудах Клаузиуса представление о том, что газовые молекулы нельзя рассматривать как отдельные материальные точки. У многоатомных молекул имеются ещё вращение молекулы как целого и колебания составляющих её атомов. Он вводит в рассмотрение число степеней свободы молекул как число «переменных, требующихся для определения положения всех составных частей молекулы в пространстве и их положения друг относительно друга» и показывает, что из данных эксперимента по теплоёмкости газов следует равномерное распределение энергии между различными степенями свободы. На каждую степень свободы приходится одна и та же энергия
Больцмана напрямую связал характеристики микромира с характеристиками макромира. Вот ключевая формула, устанавливающая это соотношение:
1/2 mv2 = kT
где m и v - соответственно масса и средняя скорость движения молекул газа, Т - температура газа (по абсолютной шкале Кельвина), а k - постоянная Больцмана. Это уравнение прокладывает мостик между двумя мирами, связывая характеристики атомного уровня (в левой части) с объемными свойствами (в правой части), которые можно измерить при помощи человеческих приборов, в данном случае термометров. Эту связь обеспечивает постоянная Больцмана k, равная 1,38 x 10-23 Дж/К.
Заканчивая разговор о постоянной Больцмана, хочется ещё раз подчеркнуть её фундаментальное значение в науке. Она содержит в себе громадные пласты физики - атомистика и молекулярно-кинетическая теория строения вещества, статистическая теория и сущность тепловых процессов. Изучение необратимости тепловых процессов раскрыло природу физической эволюции, сконцентрировавшейся в формуле Больцмана S=klnW. Следует подчеркнуть, что положение, согласно которому замкнутая система рано или поздно придёт в состояние термодинамического равновесия, справедливо лишь для изолированных систем и систем, находящихся в стационарных внешних условиях. В нашей Вселенной непрерывно происходят процессы, результатом которых является изменение её пространственных свойств. Нестационарность Вселенной неизбежно приводит к отсутствию в ней статистического равновесия.
План:
-
Введение
- 1 Связь между температурой и энергией
- 2 Определение энтропии Примечания
Введение
Постоянная Больцмана (k или k B ) - физическая постоянная, определяющая связь между температурой и энергией. Названа в честь австрийского физика Людвига Больцмана, сделавшего большой вклад в статистическую физику, в которой эта постоянная играет ключевую роль. Её экспериментальное значение в системе СИ равно
Дж/К .
Числа в круглых скобках указывают стандартную погрешность в последних цифрах значения величины. Постоянная Больцмана может быть получена из определения абсолютной температуры и других физических постоянных. Однако, вычисление постоянной Больцмана с помощью основных принципов слишком сложно и невыполнимо при современном уровне знаний. В естественной системе единиц Планка естественная единица температуры задаётся так, что постоянная Больцмана равна единице.
Универсальная газовая постоянная определяется как произведение постоянной Больцмана на число Авогадро, R = k N A . Газовая постоянная более удобна, когда число частиц задано в молях.
1. Связь между температурой и энергией
В однородном идеальном газе, находящемся при абсолютной температуре T , энергия, приходящаяся на каждую поступательную степень свободы, равна, как следует из распределения Максвелла k T / 2 . При комнатной температуре (300 К) эта энергия составляет Дж, или 0,013 эВ. В одноатомном идеальном газе каждый атом обладает тремя степенями свободы, соответствующими трём пространственным осям, что означает, что на каждый атом приходится энергия в .
Зная тепловую энергию, можно вычислить среднеквадратичную скорость атомов, которая обратно пропорциональна квадратному корню атомной массы. Среднеквадратичная скорость при комнатной температуре изменяется от 1370 м/с для гелия до 240 м/с для ксенона. В случае молекулярного газа ситуация усложняется, например двухатомный газ уже имеет приблизительно пять степеней свободы.
2. Определение энтропии
Энтропия термодинамической системы определяется как натуральный логарифм от числа различных микросостояний Z , соответствующих данному макроскопическому состоянию (например, состоянию с заданной полной энергией).
S = k lnZ .Коэффициент пропорциональности k и есть постоянная Больцмана. Это выражение, определяющее связь между микроскопическими (Z ) и макроскопическими состояниями (S ), выражает центральную идею статистической механики.
Примечания
- 1 2 3 http://physics.nist.gov/cuu/Constants/Table/allascii.txt - physics.nist.gov/cuu/Constants/Table/allascii.txt Fundamental Physical Constants - Complete Listing
Данный реферат составлен на основе статьи из русской Википедии . Синхронизация выполнена 10.07.11 01:04:29
Похожие рефераты:
Постоя́нная Бо́льцмана ( или ) - физическая постоянная , определяющая связь между температурой и энергией . Названа в честь австрийского физика Людвига Больцмана , сделавшего большой вклад в статистическую физику , в которой эта постоянная играет ключевую роль. Её экспериментальное значение в Международной системе единиц (СИ) равно:
Дж / .
Числа в круглых скобках указывают стандартную погрешность в последних цифрах значения величины. В естественной системе единиц Планка естественная единица температуры задаётся так, что постоянная Больцмана равна единице.
Связь между температурой и энергией
В однородном идеальном газе , находящемся при абсолютной температуре , энергия, приходящаяся на каждую поступательную степень свободы , равна, как следует из распределения Максвелла , . При комнатной температуре (300 ) эта энергия составляет Дж , или 0,013 эВ . В одноатомном идеальном газе каждый атом обладает тремя степенями свободы, соответствующими трём пространственным осям, что означает, что на каждый атом приходится энергия в .
Зная тепловую энергию, можно вычислить среднеквадратичную скорость атомов, которая обратно пропорциональна квадратному корню атомной массы. Среднеквадратичная скорость при комнатной температуре изменяется от 1370 м/с для гелия до 240 м/с для ксенона . В случае молекулярного газа ситуация усложняется, например, двухатомный газ имеет пять степеней свободы (при низких температурах, когда не возбуждены колебания атомов в молекуле).
Определение энтропии
Энтропия термодинамической системы определяется как натуральный логарифм от числа различных микросостояний , соответствующих данному макроскопическому состоянию (например, состоянию с заданной полной энергией).
Коэффициент пропорциональности и есть постоянная Больцмана. Это выражение, определяющее связь между микроскопическими () и макроскопическими состояниями (), выражает центральную идею статистической механики.
Предполагаемая фиксация значения
XXIV Генеральная конференция по мерам и весам , состоявшаяся 17-21 октября 2011 года, приняла резолюцию , в которой, в частности, предложено будущую ревизию Международной системы единиц произвести так, чтобы зафиксировать значение постоянной Больцмана, после чего она будет считаться определённой точно . В результате будет выполняться точное равенство k =1,380 6X·10 −23 Дж/К . Такая предполагаемая фиксация связана со стремлением переопределить единицу термодинамической температуры кельвин , связав его величину со значением постоянной Больцмана.
См. также
Напишите отзыв о статье "Постоянная Больцмана"
Примечания
| Это заготовка статьи по термодинамике и статистической физике . Вы можете помочь проекту, дополнив её. |
Отрывок, характеризующий Постоянная Больцмана
– Но что же это значит? – задумчиво сказала Наташа.– Ах, я не знаю, как все это необычайно! – сказала Соня, хватаясь за голову.
Через несколько минут князь Андрей позвонил, и Наташа вошла к нему; а Соня, испытывая редко испытанное ею волнение и умиление, осталась у окна, обдумывая всю необычайность случившегося.
В этот день был случай отправить письма в армию, и графиня писала письмо сыну.
– Соня, – сказала графиня, поднимая голову от письма, когда племянница проходила мимо нее. – Соня, ты не напишешь Николеньке? – сказала графиня тихим, дрогнувшим голосом, и во взгляде ее усталых, смотревших через очки глаз Соня прочла все, что разумела графиня этими словами. В этом взгляде выражались и мольба, и страх отказа, и стыд за то, что надо было просить, и готовность на непримиримую ненависть в случае отказа.
Соня подошла к графине и, став на колени, поцеловала ее руку.
– Я напишу, maman, – сказала она.
Соня была размягчена, взволнована и умилена всем тем, что происходило в этот день, в особенности тем таинственным совершением гаданья, которое она сейчас видела. Теперь, когда она знала, что по случаю возобновления отношений Наташи с князем Андреем Николай не мог жениться на княжне Марье, она с радостью почувствовала возвращение того настроения самопожертвования, в котором она любила и привыкла жить. И со слезами на глазах и с радостью сознания совершения великодушного поступка она, несколько раз прерываясь от слез, которые отуманивали ее бархатные черные глаза, написала то трогательное письмо, получение которого так поразило Николая.
На гауптвахте, куда был отведен Пьер, офицер и солдаты, взявшие его, обращались с ним враждебно, но вместе с тем и уважительно. Еще чувствовалось в их отношении к нему и сомнение о том, кто он такой (не очень ли важный человек), и враждебность вследствие еще свежей их личной борьбы с ним.
Но когда, в утро другого дня, пришла смена, то Пьер почувствовал, что для нового караула – для офицеров и солдат – он уже не имел того смысла, который имел для тех, которые его взяли. И действительно, в этом большом, толстом человеке в мужицком кафтане караульные другого дня уже не видели того живого человека, который так отчаянно дрался с мародером и с конвойными солдатами и сказал торжественную фразу о спасении ребенка, а видели только семнадцатого из содержащихся зачем то, по приказанию высшего начальства, взятых русских. Ежели и было что нибудь особенное в Пьере, то только его неробкий, сосредоточенно задумчивый вид и французский язык, на котором он, удивительно для французов, хорошо изъяснялся. Несмотря на то, в тот же день Пьера соединили с другими взятыми подозрительными, так как отдельная комната, которую он занимал, понадобилась офицеру.
Все русские, содержавшиеся с Пьером, были люди самого низкого звания. И все они, узнав в Пьере барина, чуждались его, тем более что он говорил по французски. Пьер с грустью слышал над собою насмешки.
На другой день вечером Пьер узнал, что все эти содержащиеся (и, вероятно, он в том же числе) должны были быть судимы за поджигательство. На третий день Пьера водили с другими в какой то дом, где сидели французский генерал с белыми усами, два полковника и другие французы с шарфами на руках. Пьеру, наравне с другими, делали с той, мнимо превышающею человеческие слабости, точностью и определительностью, с которой обыкновенно обращаются с подсудимыми, вопросы о том, кто он? где он был? с какою целью? и т. п.
Вопросы эти, оставляя в стороне сущность жизненного дела и исключая возможность раскрытия этой сущности, как и все вопросы, делаемые на судах, имели целью только подставление того желобка, по которому судящие желали, чтобы потекли ответы подсудимого и привели его к желаемой цели, то есть к обвинению. Как только он начинал говорить что нибудь такое, что не удовлетворяло цели обвинения, так принимали желобок, и вода могла течь куда ей угодно. Кроме того, Пьер испытал то же, что во всех судах испытывает подсудимый: недоумение, для чего делали ему все эти вопросы. Ему чувствовалось, что только из снисходительности или как бы из учтивости употреблялась эта уловка подставляемого желобка. Он знал, что находился во власти этих людей, что только власть привела его сюда, что только власть давала им право требовать ответы на вопросы, что единственная цель этого собрания состояла в том, чтоб обвинить его. И поэтому, так как была власть и было желание обвинить, то не нужно было и уловки вопросов и суда. Очевидно было, что все ответы должны были привести к виновности. На вопрос, что он делал, когда его взяли, Пьер отвечал с некоторою трагичностью, что он нес к родителям ребенка, qu"il avait sauve des flammes [которого он спас из пламени]. – Для чего он дрался с мародером? Пьер отвечал, что он защищал женщину, что защита оскорбляемой женщины есть обязанность каждого человека, что… Его остановили: это не шло к делу. Для чего он был на дворе загоревшегося дома, на котором его видели свидетели? Он отвечал, что шел посмотреть, что делалось в Москве. Его опять остановили: у него не спрашивали, куда он шел, а для чего он находился подле пожара? Кто он? повторили ему первый вопрос, на который он сказал, что не хочет отвечать. Опять он отвечал, что не может сказать этого.
Согласно закону Стефана – Больцмана плотность интегрального полусферического излучения E 0 зависит только от температуры и изменяется пропорционально четвертой степени абсолютной температуры T :
Стефана – Больцмана постоянная σ 0 – физическая постоянная, входящая в закон, определяющий объемную плотность равновесного теплового излучения абсолютно черного тела:

Исторически закон Стефана-Больцмана был сформулирован раньше закона излучения Планка, из которого он вытекает как следствие. Закон Планка устанавливает зависимость спектральной плотности потока излучения E 0 от длины волны λ и температуры T :

где λ – длина волны, м; с
=2,998 10 8 м/с – скорость
света в вакууме; Т
– температура тела, К;
h
= 6,625 ×10 -34 Дж×с– постоянная Планка.
Физическая постоянная k , равная отношению универсальной газовой постоянной R =8314Дж/(кг× K) к числу Авогадро NA =6,022× 10 26 1/(кг× моль):

Число различных конфигураций системы из N частиц для данного набора чисел n i (число частиц, находящихся в i -том состоянии, которому соответствует энергия e i ) пропорционально величине:

Величина W есть число способов распределения N частиц по энергетическим уровням. Если справедливо соотношение (6) то считается, что исходная система подчиняется статистике Больцмана. Набор чисел n i , при котором число W максимально, встречается наиболее часто и соответствует наиболее вероятному распределению.
Физическая кинетика – микроскопическая теория процессов в статистически неравновесных системах.
Описание большого числа частиц может успешно осуществляться вероятностными методами. Для одноатомного газа состояние совокупности молекул определяется их координатами и значениями проекций скоростей на соответствующие координатные оси. Математически это описывается функцией распределения, характеризующей вероятность пребывания частицы в данном состоянии:

есть ожидаемое число молекул в объеме d d , координаты которых находятся в интервале от до +d , а скорости в интервале от до +d.
Если осредненной по времени потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией, то газ называется идеальным. Идеальный газ называется газом Больцмана, если отношение длины пробега молекул в этом газе к характерному размеру течения L конечно, т.е.

т.к. длина пробега обратно пропорциональна nd 2 (n – числовая плотность 1/м 3 , d – диаметр молекулы, м).
Величину
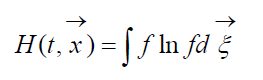
называют H -функцией Больцмана для единицы объема, которая связана с вероятностью обнаружения системы из молекул газа в данном состоянии. Каждому состоянию соответствуют определенные числа заполнения шестимерных пространственно-скоростных ячеек, на которые может быть разбито фазовое пространство рассматриваемых молекул. Обозначим W вероятность того, что в первой ячейке рассматриваемого пространства окажется N 1 молекул, во второй N 2 и т.д.
С точностью до постоянной, определяющей начало отсчета вероятности, правомерно соотношение:
 ,
,
где 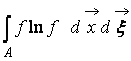 – H-функция области
пространства А
, занятой газом. Из (9) видно, что W
и H
взаимосвязаны, т.е. изменение вероятности состояния приводит к соответствующей
эволюции H функции.
– H-функция области
пространства А
, занятой газом. Из (9) видно, что W
и H
взаимосвязаны, т.е. изменение вероятности состояния приводит к соответствующей
эволюции H функции.

Больцмана принцип устанавливает связь между энтропией S физической системы и термодинамической вероятностью W её состояния:

(печатается по изданию: Коган М.Н. Динамика разреженного газа. – М.: Наука, 1967.)
Общий вид КУБ:

где – массовая сила, обусловленная наличием различных полей (гравитационного, электрического, магнитного), действующая на молекулу; J – интеграл столкновений. Именно этот член уравнения Больцмана учитывает столкновения молекул друг с другом и соответствующие изменения скоростей взаимодействующих частиц. Интеграл столкновений представляет собой пятимерный интеграл и имеет следующую структуру:

Уравнение (12) с интегралом (13) получено для столкновения молекул, при которых не возникает тангенциальных сил, т.е. сталкивающиеся частицы считаются идеально гладкими.
В процессе
взаимодействия внутренняя энергия молекул не меняется, т.е. предполагается, что
эти молекулы являются идеально упругими. Рассматриваются две группы молекул,
имеющих до соударения друг с другом (столкновения) скорости и (рис. 1), а после
столкновения соответственно скорости и . Разность скоростей и называется
относительной скоростью, т.е. . Ясно, что для гладкого упругого
столкновения .
Функции распределения f 1 ", f", f 1 ,f
описывают
молекулы соответствующих групп после и до столкновений, т.е. ![]() ;
; ![]() ;
; ![]() ;
; ![]() .
.

Рис. 1. Столкновение двух молекул.
В (13) входят два параметра, характеризующие расположение сталкивающихся молекул друг относительно друга: b и ε; b – прицельное расстояние, т.е. наименьшее расстояние, на которое сблизились бы молекулы при отсутствии взаимодействия (рис. 2); ε называют угловым параметром столкновений (рис. 3). Интегрирование по b от 0 до ¥ и по от 0 до 2p (два внешних интеграла в (12)) охватывает всю плоскость силового взаимодействия перпендикулярно вектору

Рис. 2. Траектория движения молекул.
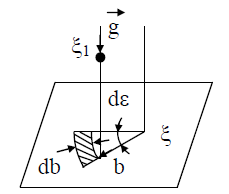
Рис. 3. Рассмотрение взаимодействия молекул в цилиндрической системе координат: z , b , ε
Кинетическое уравнение Больцмана выведено при следующих допущениях и предположениях.
1. Считается, что происходит в основном столкновения двух молекул, т.е. роль столкновений одновременно трех и большего числа молекул незначительна. Это допущение позволяет использовать для анализа одночастичную функцию распределения, которая выше названа просто функцией распределения. Учет столкновения трех молекул приводит к необходимости использования в исследовании двухчастичной функции распределения. Соответственно анализ существенно усложняется.
2. Предположение о молекулярном хаосе. Оно выражается в том, что вероятности обнаружения частицы 1 в фазовой точке и частицы 2 в фазовой точке независимы друг от друга.
3.
Равновероятны столкновения молекул с любым прицельным расстоянием, т.е. функция
распределения не меняется на диаметре взаимодействия. Необходимо отметить, что
анализируемый элемент должен быть малым, чтобы f
в пределах этого элемента не менялась, но в то же время
чтобы
не была велика относительная флуктуация ~
. Потенциалы
взаимодействия, используемые при вычислении интеграла столкновений, являются
сферически симметричными, т.е. ![]() .
.
Распределение Максвелла-Больцмана
Равновесное состояние газа описывается абсолютным Максвелловским распределением, которое является точным решением кинетического уравнения Больцмана:

где m – масса молекулы, кг.
Общее локально-максвелловское распределение иначе называемое распределение Максвелла-Больцмана:

в том случае, когда газ движется
как целое со скоростью и переменные n
,
T
зависят от координаты
и времени t
.
В поле тяготения Земли точное решение уравнения Больцмана показывает:

где n 0 = плотность у поверхности Земли, 1/м 3 ; g – ускорение силы тяжести, м/с 2 ; h – высота, м. Формула (16) является точным решением кинетического уравнения Больцман либо в безграничном пространстве, либо при наличии границ, не нарушающих этого распределения, при этом температура также должна оставаться постоянной.
Эта страница оформлена Пузиной Ю.Ю. при поддержке Российского Фонда Фундаментальных Исследований – проект №08-08-00638.


